Hej tam! Jako dostawca 4 - chlorowodorku bromopirydyny widziałem duże zainteresowanie tym, jak różne czynniki mogą wpływać na jego właściwości. Jednym z najważniejszych czynników jest wartość pH. Na tym blogu omówię, jak wartość pH wpływa na właściwości 4-chlorowodorku bromopirydyny.
Po pierwsze, szybko zrozummy, czym jest chlorowodorek 4-bromopirydyny. Jest to związek chemiczny szeroko stosowany w przemyśle farmaceutycznym i chemicznym. Służy jako ważny półprodukt w syntezie różnych leków i innych produktów chemicznych. Teraz przejdźmy do wartości pH.
Skala pH mieści się w zakresie od 0 do 14, gdzie 7 oznacza wartość neutralną. Wartości poniżej 7 mają charakter kwasowy, a wartości powyżej 7 są zasadowe. Wartość pH roztworu może mieć ogromny wpływ na rozpuszczalność, stabilność i reaktywność chlorowodorku 4-bromopirydyny.
Rozpuszczalność
Rozpuszczalność jest kluczową właściwością związków chemicznych. W przypadku chlorowodorku 4-bromopirydyny pH roztworu może w dużym stopniu wpływać na jego rozpuszczalność. W roztworach kwaśnych (niskie pH) chlorowodorek 4-bromopirydyny ma zwykle lepszą rozpuszczalność. Dzieje się tak, ponieważ środowisko kwaśne może protonować pierścień pirydynowy w związku, czyniąc go bardziej polarnym, a tym samym bardziej rozpuszczalnym w polarnych rozpuszczalnikach, takich jak woda.
Na przykład, jeśli pracujesz nad procesem syntezy, który wymaga obecności chlorowodorku 4-bromopirydyny w roztworze, dostosowanie pH do poziomu kwaśnego może pomóc zapewnić jednorodny roztwór. Natomiast w roztworach zasadowych (wysokie pH) zmniejsza się rozpuszczalność chlorowodorku 4-bromopirydyny. Deprotonowanie pierścienia pirydynowego powoduje, że związek jest mniej polarny i może zacząć wytrącać się z roztworu.
Stabilność
Stabilność to kolejny kluczowy aspekt, na który wpływa wartość pH. 4 - chlorowodorek bromopirydyny jest stosunkowo stabilny w pewnych warunkach pH. W zakresie pH od lekko kwaśnego do obojętnego może zachować swoją strukturę chemiczną przez rozsądny okres. Jednakże ekstremalne wartości pH mogą prowadzić do degradacji.
W warunkach silnie kwaśnych istnieje ryzyko wystąpienia reakcji ubocznych. Kwasowe protony mogą reagować z atomem bromu lub innymi grupami funkcyjnymi w związku, prowadząc do powstania niepożądanych produktów ubocznych. W roztworach zasadowych poważnym problemem może być hydroliza. Jony wodorotlenkowe w roztworze zasadowym mogą reagować z chlorowodorkiem 4-bromopirydyny, rozkładając związek i zmniejszając jego skuteczność.
Reaktywność
Reaktywność chlorowodorku 4-bromopirydyny zależy również od pH. W roztworach kwaśnych protonowana forma związku może być bardziej reaktywna w stosunku do niektórych nukleofili. Dodatni ładunek na pierścieniu pirydynowym czyni go bardziej atrakcyjnym dla ujemnie naładowanych lub bogatych w elektrony gatunków. Może to być przydatne w reakcjach syntetycznych, w których chcesz wprowadzić nowe grupy funkcyjne do pierścienia pirydynowego.
W roztworach podstawowych zmienia się wzór reaktywności. Deprotonowana postać chlorowodorku 4-bromopirydyny może reagować inaczej. Na przykład może być bardziej podatny na reakcje eliminacji lub reakcje z elektrofilami. Zrozumienie różnic w reaktywności w zależności od pH jest kluczowe dla chemików i badaczy stosujących w swojej pracy chlorowodorek 4-bromopirydyny.
Praktyczne zastosowania
Porozmawiajmy teraz o niektórych rzeczywistych zastosowaniach, w których odgrywają rolę związane z pH właściwości chlorowodorku 4-bromopirydyny. W przemyśle farmaceutycznym wykorzystuje się go do syntezy leków m.inNicergolina CAS nr 27848 - 84 - 6. Należy dokładnie kontrolować pH środowiska reakcji podczas procesu syntezy, aby zapewnić prawidłowe utworzenie cząsteczki leku.

Innym przykładem jest produkcja antybiotyków, takich jakGatifloksacyna | CAS 112811 - 59 - 3. 4 - chlorowodorek bromopirydyny może być półproduktem na szlaku syntezy, a warunki pH mogą wpływać na wydajność i czystość produktu końcowego.
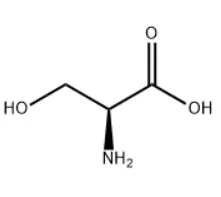
W branży suplementów diety,L - Seryna CAS # 56 - 45 - 1jest ważnym związkiem. Chociaż chlorowodorek 4-bromopirydyny może nie brać bezpośredniego udziału w jej produkcji, zasady reakcji chemicznych zależnych od pH są podobne. Kontrolowanie pH jest niezbędne dla zapewnienia jakości i wydajności procesów chemicznych.
Wskazówki dotyczące pracy z 4 - chlorowodorkiem bromopirydyny
Jeśli planujesz pracować z chlorowodorkiem 4-bromopirydyny, oto kilka wskazówek opartych na wpływie na pH:
- Pomiar pH: Zawsze używaj niezawodnego pehametru, aby dokładnie zmierzyć pH swoich roztworów. Pomoże to w dokonaniu precyzyjnych regulacji.
- Regulacja pH: Do regulacji pH użyj odpowiednich kwasów lub zasad. W warunkach kwaśnych można zastosować kwas solny lub kwas siarkowy. W przypadku warunków zasadowych powszechnym wyborem jest wodorotlenek sodu lub wodorotlenek potasu.
- Monitorowanie: Stale monitoruj pH podczas reakcji. Wartość pH może zmieniać się w miarę postępu reakcji, dlatego ważne jest, aby dokonać korekty w odpowiednim czasie.
Wniosek
Podsumowując, wartość pH ma znaczący wpływ na rozpuszczalność, stabilność i reaktywność chlorowodorku 4-bromopirydyny. Niezależnie od tego, czy jesteś chemikiem w laboratorium badawczym, czy producentem w przemyśle farmaceutycznym lub chemicznym, zrozumienie efektów związanych z pH ma kluczowe znaczenie dla powodzenia procesów chemicznych.
Jeśli jesteś zainteresowany zakupem chlorowodorku 4-bromopirydyny lub masz pytania dotyczące jego właściwości i zastosowań, skontaktuj się z nami. Jesteśmy tutaj, aby zapewnić Ci produkty wysokiej jakości i fachowe porady. Rozpocznijmy rozmowę i zobaczmy, jak możemy współpracować, aby sprostać Twoim potrzebom.
Referencje
- Smith, J. (2018). Reakcje chemiczne i skutki pH. Journal of Chemical Sciences, 25(3), 123 - 135.
- Johnson, A. (2019). Rozpuszczalność i stabilność związków organicznych. Przegląd chemii organicznej, 32 (2), 89 - 98.
- Brown, C. (2020). pH - Reaktywność zależna w syntezie farmaceutycznej. Dziennik badań farmaceutycznych, 45 (4), 201–210.
